La campanya de vacunació contra la Covid-19 començarà abans del que estava previst a Europa. L'Agència Europea del Medicament (EMA) ha avançat al 21 de desembre la reunió per avaluar la vacuna de Pfizer-BioNTech, que podria autoritzar aquell mateix dia.
L'Agència Europea del Medicament ha anunciat aquest dimarts al migdia que el seu comitè d'experts ha decidit reunir-se dilluns de la setmana que ve després de rebre "informació addicional" de les farmacèutiques sobre la vacuna. El regulador de la Unió Europea, es cura en salut, i no garanteix que el dia 21 prengui una decisió. Per això, manté la trobada del dia 29 que estava prevista en un inici. "Acabarem l'avaluació tan aviat com es pugui i només quan les dades sobre la qualitat, la seguretat i l'eficàcia de la vacuna siguin prou sòlides i completes per determinar si els beneficis de la vacuna superen els seus riscos", ha recordat l'EMA.
Pressions
Les darreres hores havien transcendit pressions de diferents governs europeus per tal que l'agència avancés la seva decisió sobre la vacuna davant l'extensió de la pandèmia registrades en els darrers dies a bona part d'Europa. I més quan altres països com ara el Regne Unit, els Estats units o el Canadà ja han començat a administrar la vacuna de Pfizer.
L'autorització per part de l'agència europea permetria avançar la campanya de vacunació. Catalunya ja té preparat el dispositiu per administrar les vacunes, que en principi s'esperava que començarien a arribar entre la primera i la segona setmana de gener. Ara, amb l'avançament de l'autorització, es podrien arribar administrar abans d'acabar l'any.

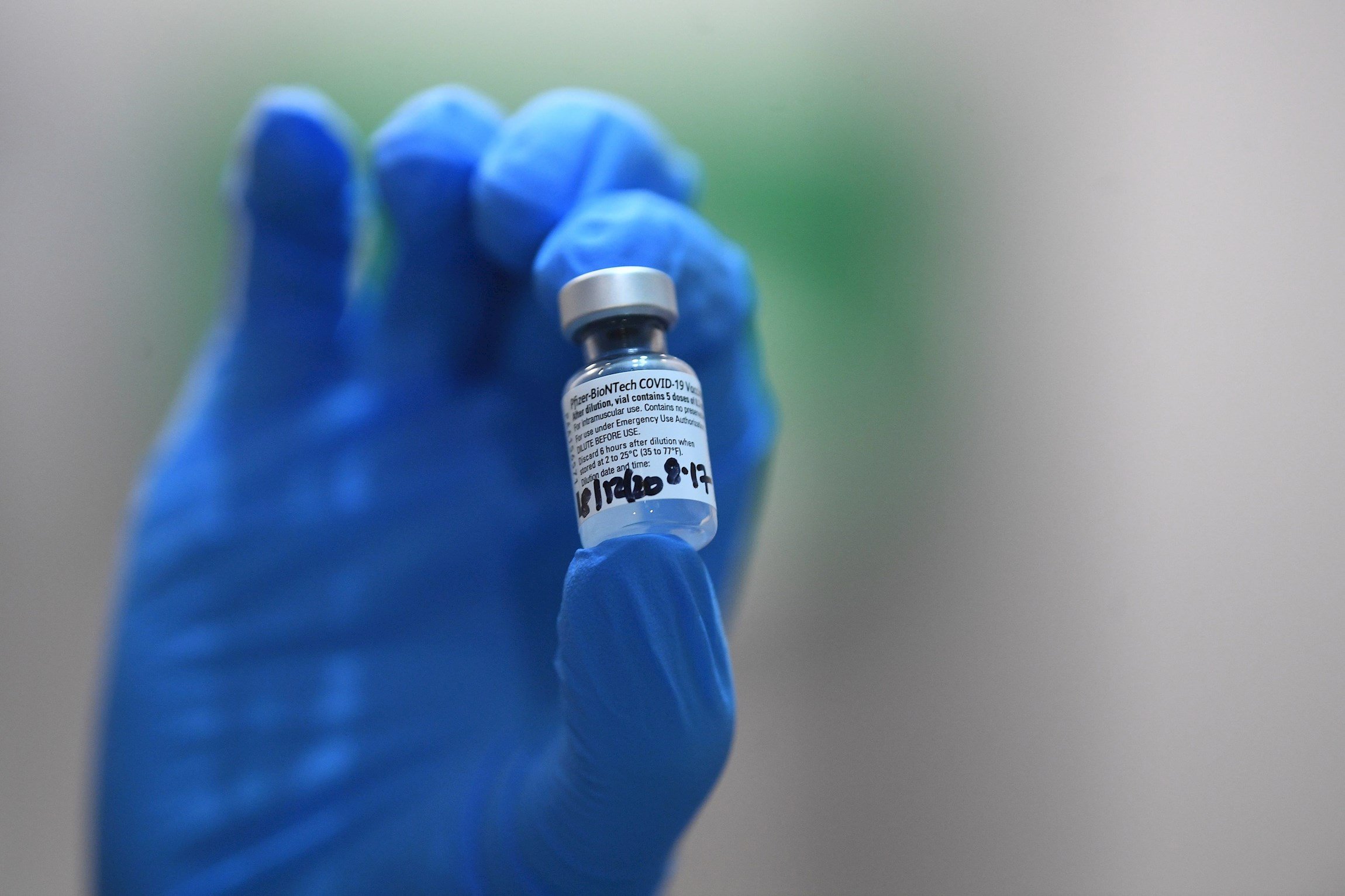
La vacuna de Pfizer-BioNTech serà la primera a rebre l'autorització a la UE / Efe
Dispositiu
La previsió del Govern era rebre en el primer trimestre de l'any que ve 900.000 dosis de la vacuna, que permetrien vacuna entre 450.000 i 500.000 persones. Només al gener s'esperava vacunar unes 150.000. L'estratègia de vacunació preveu començar a vacunar inicialment els grups d'extraordinària prioritat: la gent gran i els professionals de les residències, el personal sanitari i les persones amb discapacitat severa. El dispositiu ja està preparat: es desplaçaran unitats mòbils fins a les residències, mentre que els professionals sanitaris es vacunaran als hospitals i centres d'assistència primària.
Pendents de l'EMA
Si el comitè d'experts de l'Agència Europa del Medicament arriba a una conclusió definitiva dilluns que ve, enviarà un informe detallat amb les seves opinions a la Comissió Europea, que es preveu que acceleri el seu procés de presa de decisions per a atorgar llavors l'autorització de comercialització vàlida en tots els països europeus en el termini d'uns dies, previsiblement abans de Nadal. La presidenta de la Comissió, Úrsula von der Leyen, es mostrava confiada que la vacunació pogués començar abans d'acabar l'any.
L'autorització, que no s'atorga en un procés d'emergència sinó després d'una avaluació en temps real de les dades que han anat oferint les farmacèutiques aquests mesos, ve acompanyada amb obligacions i controls als quals s'hauran de comprometre les empreses distribuïdores de la vacuna per a complir els “alts estàndards” de la UE per a vacunes i medicaments en general. Entre les condicions que imposa la EMA està el pla de recerca per al seu ús en nens, un programa sòlid de gestió de riscos, un seguiment de la seguretat del fàrmac, així com instruccions detallades per a un ús segur.
Imatge principal, una dosi de la vacuna de Pfizer-BioNTech / Efe