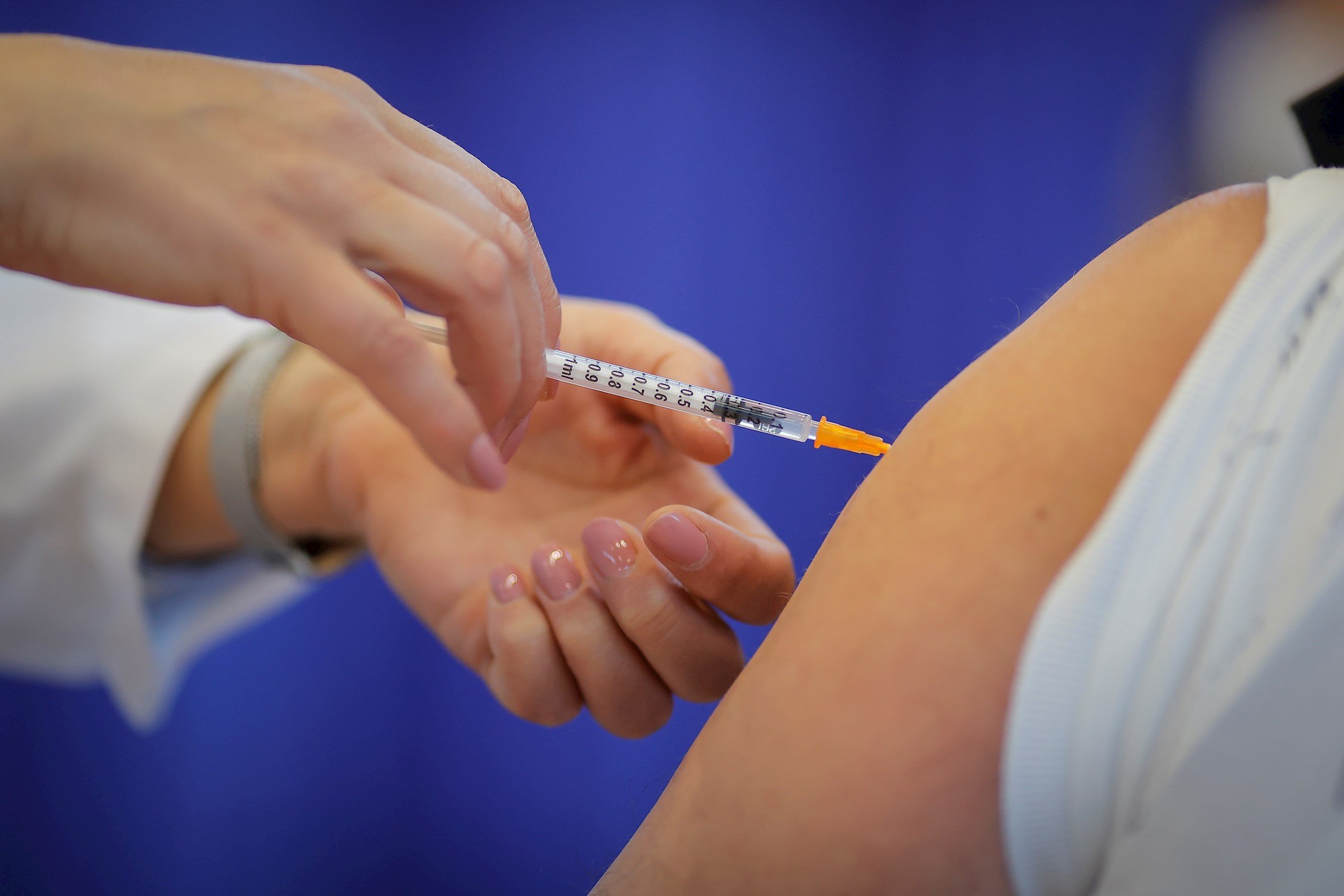
Los menores de 60 años que han recibido una primera dosis de AstraZeneca y no quieran la segunda de Pfizer tienen que firmar un protocolo de consentimiento informado. En este, se debe mostrar su rechazo a recibir una vacuna diferente y su petición expresa repetir con esta, manifestando conocer los riesgos que eso comporta.
Así lo ha avalado el Comité de Bioética de España (CBE) en respuesta a la consulta que le remitió el pasado miércoles el ministerio de Sanidad para conocer su opinión sobre si es correcto, desde el punto de vista ético, completar la pauta a estos pacientes con el suero anglosajón y, en este caso, si tenía que estar bajo consentimiento informado.
De esta manera, Sanidad ha incorporado una nota a la séptima actualización de la estrategia de vacunación con esta posibilidad y un anexo con una propuesta del formulario que tendrán que completar.
Un informe no vinculante
Cabe decir que el informe no es vinculante, dado que no se trata de un órgano decisorio, sino un órgano independiente meramente consultivo.
En el texto, se recuerda la notificación a las últimas semanas de algunos casos de trombosis de grandes vasos sanguíneos, a nivel cerebral y abdominal (síndrome de trombosis con trombocitopenia) que, "si bien son muy infrecuentes, también se consideran graves" y que "parecen incrementarse a medida que disminuye la edad".
Dos millones de ciudadanos
Fue por eso que el pasado 8 de abril España desaconsejó Vaxzevria (nombre comercial de AstraZeneca) para los menores de 60 años, lo cual dejó en el limbo las segundas dosis de los casi dos millones de ciudadanos que recibieron desde febrero una primera inyección de este preparado.
Después de ampliar para este grupo el intervalo entre dosis de 12 a 16 semanas mientras se recopilaba más evidencia científica sobre la eficacia y seguridad de administrar una pauta heteróloga, la Comisión de Salud Pública decidió el martes pasado que se les pinchara una segunda inyección de Pfizer.
"El suero no puede ser a demanda de los individuos"
El CBE ha argumentado la validación del informe diciendo que el actual contexto de la pandemia, "en la que todavía no disponemos de dosis de vacunas" para vacunar toda la población, el suero a administrar no puede ser a demanda o elección de los individuos, "bajo pena de socavar los principios y valores éticos y legales que rigen la Estrategia de vacunación contra la Covid-19".
Por lo tanto, con todos estos datos, los pacientes mayoritariamente trabajadores esenciales por debajo de los 55 años, tendrán que decidir si completan la pauta con Pfizer o, por el contrario, se niegan y, en este caso, tendrán que firmar de forma obligada el consentimiento informado.
¿Cómo debe ser el consentimiento?
Los interesados tendrán que expresar por escrito esta negativa, que quedaría registrada de la siguiente manera:
"Como Usted ha expresado su rechazo a vacunar con Comirnaty, de Pfizer / BioNTech, en la segunda dosis, y para evitar los riesgos que para su salud y la salud de la colectividad tendría no completar las dos dosis de vacuna que están pautadas, y conforme a lo que dispone el artículo 2 de la Ley 41/2002, el apartado 4 establece que la negativa al tratamiento por el paciente o usuario constará por escrito".
Además de este rechazo a recibir un fármaco diferente del de AstraZeneca, el paciente tiene que expresar su "petición de ser vacunado con una segunda dosis de Vaxzevria", manifestando, en más, "ser conocedor del infrecuente riesgo de desarrollar un síndrome de trombosis con trombocitopenia".
Esta opción tendría que venir soportada, como garantía, por un consentimiento que acredite, fundamentalmente, que el individuo rechaza, sin que se exija explicar o argumentar las razones, ser vacunado con segunda dosis de la vacuna de ARN y que solo aceptaría que le administraran la segunda dosis con el fármaco de AstraZeneca, conociendo y aceptando el riesgo del síndrome.
Una decisión que corresponde a las autoridades públicas
El CBS considera, "desde una perspectiva ética-legal", que las decisiones relacionadas con la aplicación de los fármacos en cada grupo de riesgo tienen que ser tomadas por las autoridades públicas, bajo el asesoramiento del grupo de Expertos, la Ponencia de Vacunas y la Comisión de Salud Pública, teniendo en cuenta tanto el número de dosis disponibles como la evolución de la pandemia.
Es por eso que, la persona que pida la segunda dosis de AstraZeneca, tiene que asumir a título particular los posibles riesgos que esta compuerta y dejar por escrito que es conocedor de estos.
Imagen principal, vacunación con el fármaco de Pfizer / EFE